Rosenfeld PJ. Anti-PDGF and age-related macular degeneration treatment : Where do we stand ? Presented at : Retina, 2017 ; Koloa, Hawaï.
Les études princeps qui ont validé l’utilisation du ranibizumab et de l’aflibercept de même que l’étude CATT comparant ces deux molécules au bevacizumab, ont montré que ces anti-VEGF permettaient d’obtenir un gain initial d’acuité visuel moyen de l’ordre de 6 à 8 lettres ETDRS. Au cours de la première année de traitement, ce gain est globalement maintenu avec un nombre d’injections intravitréennes de l’ordre de 5 à 6. Toutes les études de “vraie vie” ou celles validant les modalités de retraitements suivant des rythmes particuliers ont montré l’importance du suivi régulier des patients, en particulier avec des contrôles en OCT. Enfin, aucune de ces études n’a permis d’envisager une occlusion définitive des néovaisseaux choroïdiens qui imposent finalement un traitement ou tout au moins un suivi “à vie”.
Cette avancée thérapeutique illustre l’efficacité du blocage de toutes les isoformes du VEGF développé au début des années 2000. Ce concept avait fait suite à celui d’un blocage partiel de l’activité anti-VEGF “pathologique” avec le pegaptamid qui bloque l’isoforme 165 du VEGF impliqué dans les processus de néovascularisation pathologique.
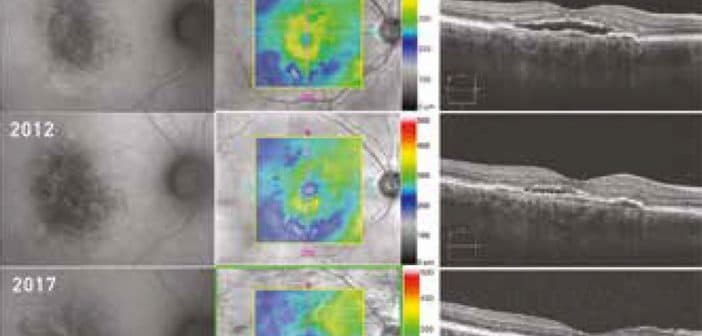
Au cours des années qui suivent la mise en route du traitement, le gain visuel initial moyen de 6 à 8 lettres ETDRS n’est pas toujours maintenu. Des processus de fibrose sous rétinienne, d’atrophie de l’épithélium pigmentaire (et de la neurorétine en regard) sont observés de même qu’une tendance à la diminution de l’observance du traitement (fig. 1). Enfin, des épisodes hémorragiques peuvent venir brutalement compromettre le pronostic visuel.
Dans ce contexte, de nombreuses molécules sont développées à la fois pour améliorer l’efficacité initiale (peut-on faire mieux que gagner 6 à 8 lettres à la fin de la phase d’induction ?) et pour améliorer la sécurité des traitements (n’est-il pas nocif de bloquer toutes les isoformes du VEGF avec un médicament injecté régulièrement dans le vitré pendant des années ?).
Les pistes des traitements à venir sont multiples. Elles ciblent le VEGF extracellulaire (VEGF-A, VEGF-B, PlGF, VEGF-C et VEGF-D) ou la cascade d’activation de la tyrosine kinase. L’angiopoïétine est une cytokine pro-angiogénique qui peut être ciblée pour réduire la prolifération néovasculaire. Une piste adjuvante concerne l’utilisation d’oligonucléotides qui ciblent le VEGF ou d’autres cytokines impliquées dans la pathogénie des néovaisseaux.
Vous êtes abonné(e)
IDENTIFIEZ-VOUS
Pas encore abonné(e)
INSCRIVEZ-VOUS
Inscrivez-vous gratuitement et profitez de tous les sites du groupe Performances Médicales
S'inscrire