
Éditorial
La génétique des maladies rétiniennes connait des avancées claires et…

La génétique des maladies rétiniennes connait des avancées claires et…

La rétinopathie diabétique (RD) est caractérisée par une occlusion des…
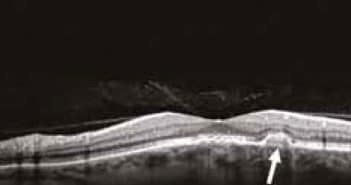
Depuis l’apparition de l’OCT-A ou OCT-angiographie, de nombreuses publications ont montré l’intérêt de cette technique dans la détection de manière non invasive des néovaisseaux choroïdiens (NVC). La myopie forte ou pathologique est associée à la survenue de néovaisseaux choroïdiens, et il est logique de voir dans cette technique, un intérêt dans la prise en charge des patients myopes forts comme c’est le cas dans la dégénérescence maculaire liée à l’âge. Force est de constater que très peu d’articles sont parus sur le sujet. Que peut-on attendre de l’OCT-A chez le myope fort ?
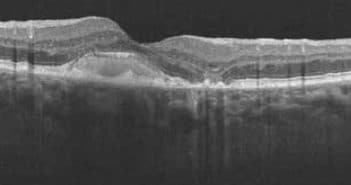
Le diagnostic des dépôts de matériel repose en partie sur l’aspect en OCT mais également sur le contexte clinique et les autres examens d’imagerie. On retiendra en particulier l’absence de DSR et l’absence d’œdème en avant de la zone ellipsoïde en OCT-B qui sont des éléments rassurants. Certains aspects restent cependant douteux tels que l’hyperréflectivité du matériel dont l’aspect peut être proche des néovaisseaux préépithéliaux (type 2) et l’aspect de pseudo-DSR sur les dépôts fragmentés avec atrophie de la rétine externe. Les DEP non vascularisés de l’EP sont une autre source de confusion. L’angiographie à la fluorescéine et l’angiographie ICG sont alors souvent contributives pour le diagnostic différentiel avec des néovaisseaux choroïdiens. L’angio-OCT apparu plus récemment est rapidement devenu l’un des éléments du diagnostic de ces dépôts de matériel en montrant l’absence de flux vasculaire en regard du dépôt. On vérifiera l’absence d’erreur de segmentation et les images de projection des vaisseaux rétiniens ne seront pas confondues avec des néovaisseaux choroïdiens. Les vaisseaux choroïdiens vus à travers les plages d’atrophie ne seront pas non plus interprétés à tort comme des lacis néovasculaires. Enfin, on prendra garde aux réels dépôts de matériel qui se compliquent de néovaisseaux choroïdiens.
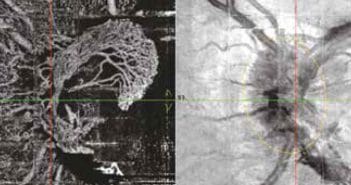
L’OCT-A est un formidable outil diagnostique et de suivi. Il vient en complément de l’imagerie habituelle (rétinographie couleur avec filtres et en auto-fluorescence, angiographie à la fluorescéine et en ICG, OCT). Pour le diagnostic, il s’agit d’une aide supplémentaire, notamment dans les diagnostics difficiles. Pour le suivi, il s’agit d’un examen de choix (systématique à mon sens) car rapide, non contact, non invasif, précis, reproductible et fiable.
Les différentes descriptions sémiologiques permettent à présent d’appréhender ces néovaisseaux de manière structurée. Les signes d’activité en OCT-A doivent être interprétés en corrélation avec les signes d’activité habituelle (DSR, logettes, DEP, hémorragies…).
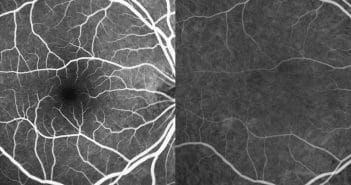
Certes, l’ophtalmologie est une spécialité “visuelle”, mais les images n’ont…

Un descemethorhexis simple consiste à retirer un certain diamètre central de la membrane de Descemet du patient receveur sans greffer un endothélium et une membrane de Descemet d’un donneur. L’idée derrière cette approche est venue de plusieurs constatations lors du suivi des patients ayant bénéficié de greffes endothéliales pures DMEK (Descemet Membrane Endothelial Keratoplasty).
D’abord, il a été noté dans le postopératoire précoce que l’éclaircissement cornéen était plus rapide en périphérie par rapport au centre cornéen. Ensuite, et en présence d’un décentrement postopératoire du greffon endothélial, la zone vierge de cellules endothéliales (entre les bords du descemethorhexis et les bords du greffon) s’éclaircissait relativement rapidement et il ne persistait pas d’œdème à ce niveau.
Enfin, dans les cas de DMEK incomplètes avec impossibilité peropératoire de positionner et/ou de dérouler le greffon endothélial, le lit stromal nu, (vierge de Descemet du fait du descemethorhexis) s’éclaircissait spontanément dans certains cas avec absence d’œdème résiduel. Ce résultat surprenant survenait lorsque l’indication opératoire était une dystrophie de Fuchs mais jamais lorsqu’il s’agissait d’une kératopathie bulleuse.
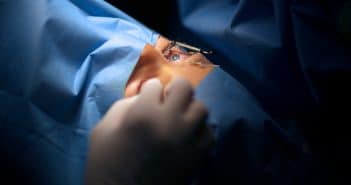
La greffe lamellaire endothéliale pure est une technique chirurgicale devenant la référence pour le traitement des dystrophies endothéliales. Il s’agit d’une technique chirurgicale délicate où la préparation du greffon est une étape essentielle. Pendant cette étape, la principale complication est la déchirure du greffon pouvant faire annuler la procédure.
En réalité, la présence d’une déchirure sur le greffon ne remet pas en cause le pronostic anatomique et fonctionnel de la greffe. Les greffons déchirés implantés ont permis une récupération identique à 6 mois avec une cinétique différente. Le greffon reste donc fonctionnel en cas de déchirure.
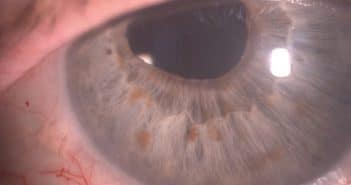
Les greffes lamellaires cornéennes sont actuellement les techniques de références pour la prise en charge chirurgicale des atteintes cornéennes endothéliales. Leur principe est relativement simple, mais les difficultés techniques rencontrées rendent la standardisation du geste difficile.
On distingue les différentes techniques en fonction de l’épaisseur du greffon avec dissection manuelle ou automatisée.
La greffe endothéliale de type DMEK est devenue la technique de référence du traitement chirurgical des dystrophies endothéliales. Les premiers résultats à long terme confirment l’excellente récupération visuelle obtenue à court terme avec une acuité visuelle moyenne à 4 ans de 20/26e soit 0.7.
Au niveau anatomique, il existe une perte régulière de cellules endothéliales qui est majorée la première année mais qui retrouve une vitesse normale dès la deuxième année avec un taux de perte d’environ 9 % par an. La DMEK est donc une chirurgie permettant une récupération rapide et durable dans le temps.
