
Quoi de neuf en Dégénérescence Maculaire Liée à l’Âge (DMLA) ?
La pathogénie de la maladie, l’imagerie, les modalités de traitements…

La pathogénie de la maladie, l’imagerie, les modalités de traitements…
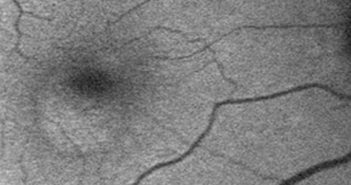
Le décollement de l’épithélium pigmentaire (DEP) est défini comme un soulèvement en dôme de l’épithélium pigmentaire (EP), qui se détache de la membrane de Bruch sous-jacente par accumulation de fluide. Il est fréquemment associé à une néovascularisation choroïdienne.
Il existe deux principales théories sur la formation des DEP : celle de Bird qui associe la formation du DEP à une augmentation de la teneur en lipides de la membrane de Bruch avec l’âge, et la théorie de Gass qui implique le développement de NVC dans l’épaisseur de la membrane de Bruch.
L’imagerie multimodale a apporté la preuve de la présence de NVC à la face postérieure d’un DEP fibrovasculaire et permet ainsi d’envisager l’hypothèse que la survenue des déchirures de l’EP en cas d’injection d’anti-VEGF est probablement liée à une rétraction du néovaisseau à la face postérieure du DEP, et ainsi responsable d’une traction sur l’EP qui provoque la déchirure.
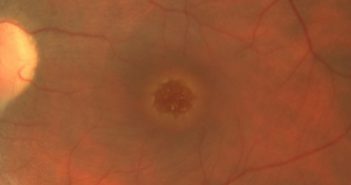
Il n’est pas toujours aisé de différencier trou maculaire (TM) et pseudo-trou maculaire (PTM) sur l’analyse du fond d’œil. L’OCT a permis de différencier ces deux entités cliniques. L’OCT “en face” permet une description précise couche par couche de l’aspect des TM et PTM qui ont des particularités anatomiques bien distinctes.
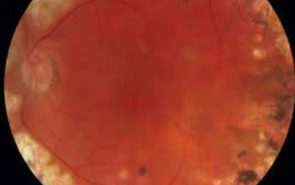
L’œdème maculaire est la principale cause de malvoyance chez les patients diabétiques. Sa prise en charge thérapeutique repose en premier lieu sur le contrôle des facteurs systémiques. Chez un certain nombre de patients cependant, un traitement ophtalmologique associé est nécessaire. À ce jour, le ranibizumab, administré en intravitréen, demeure le seul traitement pharmacologique à avoir l’AMM et le remboursement dans cette indication, mais d’autres molécules arrivent sur le marché. Parmi celles-ci, les corticoïdes à libération prolongée semblent constituer une alternative de choix car ils ciblent les différents mécanismes physiopathogéniques de l’OM diabétique et non exclusivement la voie du VEGF.
L’implant de dexaméthasone, utilisé depuis de nombreuses années dans les occlusions veineuses et les uvéites non infectieuses, semble offrir une efficacité comparable à celle du ranibizumab en termes de gain d’acuité visuelle et permet une réduction significative de l’épaisseur rétinienne. Le nombre d’injections nécessaires pour atteindre ce résultat est moindre qu’avec le ranibizumab, autorisant donc un suivi moins strict, même si un contrôle régulier de la pression oculaire reste recommandé.
Outre le risque faible de survenue d’une endophtalmie, les traitements par anti-VEGF des néovaisseaux de la DMLA pourraient comporter un risque de majoration d’une atrophie géographique (AG) [1].
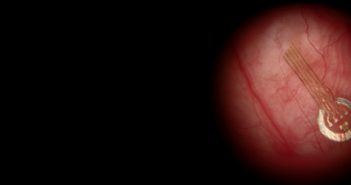
D’un simple concept au début des années 1990, la stimulation rétinienne des patients aveugles par dégénérescence des photorécepteurs est devenue une réalité. Plusieurs systèmes d’implants sous-rétiniens et prérétiniens sont sortis des laboratoires pour atteindre le stade des essais cliniques multicentriques, voire de la commercialisation.
Les résultats sont modestes dans l’absolu, mais permettent cependant d’améliorer l’autonomie de certains aveugles profonds, avec un retentissement significatif sur la qualité de vie. Le seul essai clinique actuellement en cours en France, celui de Pixium Vision, devrait confirmer les résultats de la stimulation prérétinienne qui a l’avantage, par rapport au système sous-rétinien, d’une relative simplicité d’implantation. Ce dernier, une fois débarrassé de la contrainte représentée par le câble d’alimentation, pourrait cependant devenir une voie d’avenir.

La comparaison des anti-VEGF disponibles pour injections intravitréennes (IVT) est confrontée à de nombreuses problématiques. Le manque d’homogénéité des études de laboratoire gêne la comparaison des constantes pharmacocinétiques ou des paramètres associés à l’efficacité du blocage du VEGF. Sur le plan clinique, l’hétérogénéité des études ne facilite pas la comparaison de l’efficacité sur des lésions similaires.
Depuis peu, la disponibilité des données du suivi à 96 semaines des études VIEW apporte quelques éléments comparatifs à travers une analyse post hoc. Enfin, l’hétérogénéité encore plus grande des néovascularisations observées en pratique clinique courante chez les patients atteints de DMLA reste un obstacle important pour une comparaison des molécules par les praticiens.
Nous avons cependant tenté de reprendre ici les quelques notions établies pour envisager un comparatif.
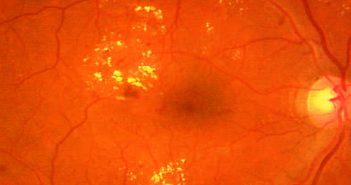
L’hypertonie oculaire après injection intravitréenne (IVT) d’implant intravitréen de corticostéroïdes est une complication potentielle nécessitant une surveillance particulière pour un dépistage et une prise en charge précoces. Jusqu’à présent, les études ont surtout été menées avec la triamcinolone en intravitréen, et les données avec l’implant de dexaméthasone sont encore à préciser.
Cette étude permet de mieux comprendre le suivi du patient post-IVT d’implant de dexaméthasone. L’objectif était d’analyser les variations de la pression intraoculaire (PIO) à court terme après IVT d’implant intravitréen de dexaméthasone afin de proposer un schéma de surveillance approprié.
Les résultats indiquent qu’il semble raisonnable d’effectuer des mesures de contrôle de la PIO à 1 et 2 mois après l’IVT. Une mesure de la PIO dans les suites immédiates de l’injection et dans les jours qui suivent (1 semaine) ne semble pas indiquée de façon systématique.
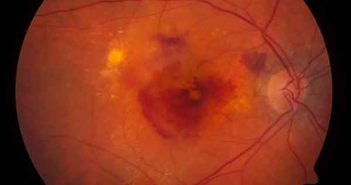
Depuis sa mise à disposition en 2007, le ranibizumab en administration intravitréenne est l’anti-VEGF le plus largement employé dans le traitement de la DMLA exsudative. L’aflibercept est un nouvel antiangiogénique ayant récemment obtenu son autorisation de mise sur le marché dans cette indication. Les schémas posologiques recommandés pour ces deux agents étant diffèrents, l’introduction de l’aflibercept pourra entraîner des modifications dans la pratique des ophtalmologistes.
Nous avons initié une étude, auprès de groupes d’ophtalmologistes de diverses régions de France, en vue :
– d’évaluer quelles sont leurs pratiques actuelles et quelles seront, selon eux, les modifications consécutives à la mise à disposition de l’aflibercept ;
– de préciser la définition qu’ils donnent d’un patient réfractaire/récidiveur dans la DMLA et leur ressenti de cette nouvelle molécule.
Il est ressorti, de ces réunions, une opinion favorable de l’efficacité de l’aflibercept et un désir, pour certains d’entre eux, de modifier leurs habitudes en matière de schéma thérapeutique.
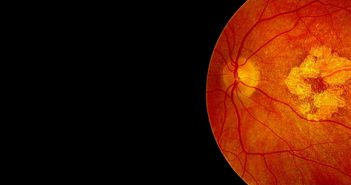
Alors que la puissance des anti-VEGF n’est plus à démontrer dans la maîtrise de la néovascularisation sous-rétinienne, leurs règles d’utilisation sont toujours l’objet de débat. Les tenants des stratégies réactives reprochant aux proactifs de surtraiter nombre de patients. Les proactifs soulignant de leur côté le caractère délétère à laisser un processus néovasculaire se réinstaller itérativement en regard ou à proximité de cellules photoréceptrices incapables de se régénérer. Au-delà d’une présentation dichotomique et partisane, à la lumière d’études récentes, une approche personnalisée peut être esquissée, qui emprunte aux deux stratégies.
