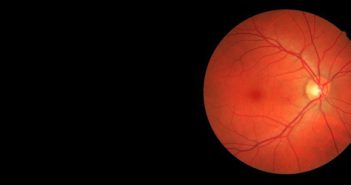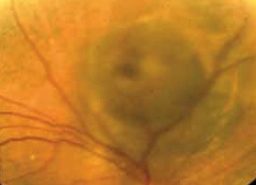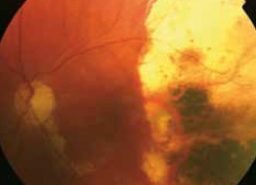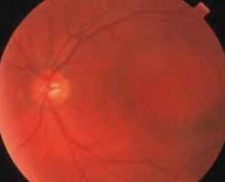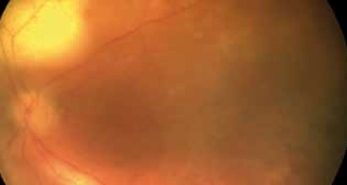
Diagnostic différentiel des pathologies rétiniennes héréditaires
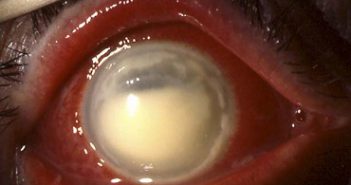
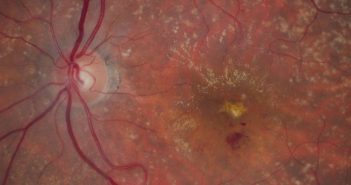
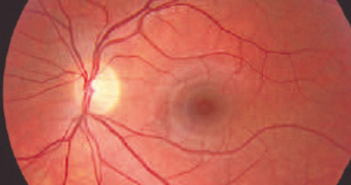
Devant une anomalie du fond d’œil, un bilan d’imagerie est réalisé de façon systématique. Un bilan d’imagerie complet permet une réflexion poussée sur l’origine du trouble. À l’ère des débuts de la thérapie génique, nous devons être capable d’évoquer une cause génétique quel que soit l’âge du patient. À l’inverse, il ne faut pas passer à côté d’une cause infectieuse, inflammatoire, iatrogène… qui pourrait alors bénéficier d’un traitement étiologique.