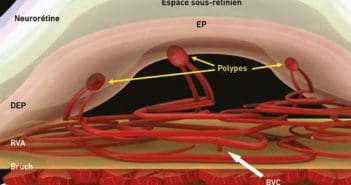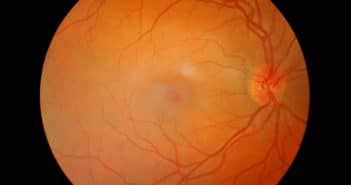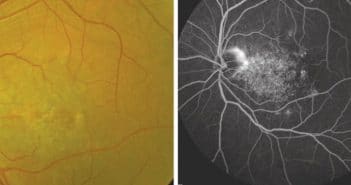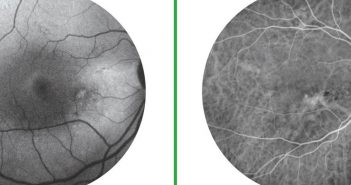
Y-a-t-il une urgence à opérer un décollement de rétine adressé un vendredi à 19 h ?
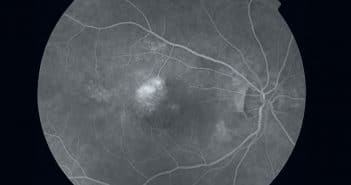
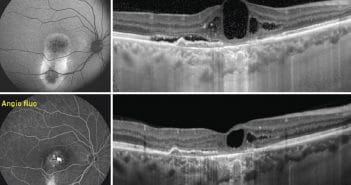
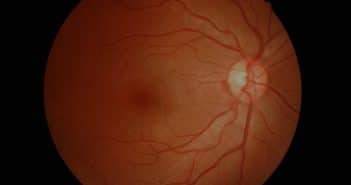
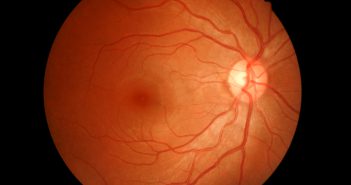
Le statut maculaire est le principal facteur déterminant le résultat fonctionnel final dans le décollement de rétine (DR) et pris en compte pour déterminer l’urgence de la prise en charge. Plusieurs études ont montré que les DR avec soulèvement maculaire avaient les mêmes résultats fonctionnels et anatomiques que la chirurgie soit réalisée dans les 3 jours ou en urgence (dans les 24 premières heures). Dans les cas de DR sans soulèvement maculaire, la chirurgie doit être réalisée en urgence, avant le décollement maculaire afin d’obtenir les meilleurs résultats visuels.
Les DR asymptomatiques par trou atrophique représentent des cas particuliers qui ne seront traités qu’en cas de progression.