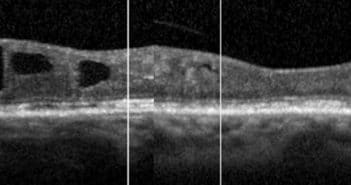
Désorganisation des couches rétiniennes internes (DRIL) et altérations vasculaires
Moein HR, Novais EA, Rebhun CB et al. OCT-Angiography to…

Moein HR, Novais EA, Rebhun CB et al. OCT-Angiography to…
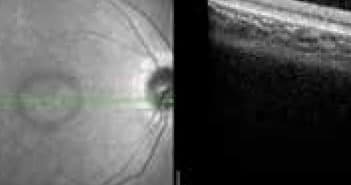
L’ophtalmologiste dans sa pratique ne voit que rarement un patient suspect ou ayant une dystrophie rétinienne. Une telle dystrophie est évoquée soit devant une histoire familiale, un signe ou tableau caractéristiques (pseudo-ostéoblastes dans les rétinites pigmentaires, dépôt vitellin large avec un pseudo-hypopion), ou faute de causes infectieuses, inflammatoires, tumorales, traumatiques, toxiques ou paranéoplasiques.
Suite à l’apparition des techniques de séquençage à haut débit (criblage simultané de plusieurs dizaines de gènes) et des thérapies géniques (choroïdérémie, rétinite pigmentaire liée à l’X et à des mutations dans le gène RPGR), l’ophtalmologiste devra désormais savoir reconnaître une dystrophie rétinienne et son mode de transmission pour argumenter le choix du panel de gènes et orienter les patients pouvant être inclus dans les protocoles de thérapie génique.
De plus, le recours aux analyses d’exome ou de génome met l’ophtalmologiste et le généticien dans la situation de pouvoir identifier fortuitement des mutations dans des gènes associés à des cancers, à des pathologies neurologiques dégénératives. Le consentement doit ainsi préciser si l’analyse et/ou l’information donnée au patient sera restreinte aux seuls gènes des dystrophies rétiniennes ou élargie à tous les gènes.

La périphérie rétinienne du patient diabétique doit être au centre de nos préoccupations tant les risques d’aggravation sont élevés et les complications sévères (hémorragies intravitréennes, décollement de rétine tractionnel, glaucome néovasculaire). Le traitement de référence de la rétinopathie diabétique proliférante est la photocoagulation panrétinienne. Mais l’avènement des anti-VEGF va peut-être modifier cette hégémonie.
En effet, les anti-VEGF semblent démontrer des performances intéressantes en termes de stabilisation ou de régression de la sévérité de la rétinopathie diabétique, ou en termes de complications liées à la rétinopathie diabétique proliférante. Cependant, ces résultats sont obtenus au prix de très nombreuses injections. S’il est encore trop tôt pour conseiller de changer de paradigme entre PRP et IVT, il est nécessaire de suivre avec attention les progrès dans ce domaine.
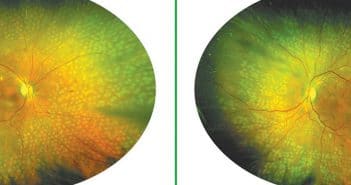
Depuis plus de 30 ans, la photocoagulation panrétinienne (PPR) reste le gold-standard dans le traitement de la rétinopathie diabétique et, hormis l’apparition des lasers multispots, le mode de réalisation des PPR n’a presque pas évolué.
Cependant, une nouvelle technologie est récemment apparue avec le laser Navilas qui permet la réalisation de laser assisté par ordinateur. Cet appareil offre la possibilité de planifier à l’avance la localisation des impacts laser que l’on souhaite effectuer et ainsi, augmenter la précision des traitements aussi bien maculaires que périphériques.
De plus, il a été montré que les séances de PPR utilisant cette technologie sont plus rapides et moins douloureuses pour le patient qu’avec un laser multispot classique.
Le laser Navilas est donc une très bonne alternative aux appareils traditionnels.
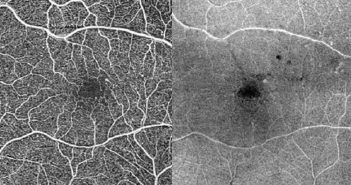
L’OCT-A permet par un examen non invasif de la rétine une analyse de la structure et de la localisation des anomalies vasculaires associées à la rétinopathie diabétique (RD) : microanévrismes, anomalies microvasculaires intrarétiniennes (AMIR), et néovaisseaux prérétiniens. De plus, grâce à de nombreux indices, il permet d’évaluer de façon quantitative la perfusion maculaire.
La plupart des études s’entendent sur le fait qu’il existe un lien entre l’état du réseau vasculaire maculaire et le stade de la RD. Les mesures de la zone avasculaire centrale (ZAC) présentent un niveau de corrélation faible avec le stade de la RD. Alors qu’il semblerait que la densité vasculaire soit davantage corrélée, même s’il existe une discordance entre les études sur la nature de l’indice le plus performant. Ces outils ne se substituent pas encore aux méthodes standardisées recommandées par la classification ETDRS (rétinographies), d’autant plus que les mesures en OCT-A ne nous fournissent pas de valeurs seuils spécifiques de chaque stade de l’ETDRS. Des avancées dans ce domaine sont donc nécessaires avant de pouvoir éventuellement classer, diagnostiquer et suivre la RD en s’affranchissant de l’évaluation du fond d’œil par rétinographie.
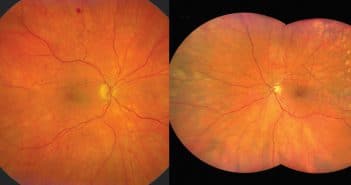
Ces dernières années ont vu se développer l’utilisation de l’imagerie ultra grand champ du fond d’œil qui s’impose progressivement dans de nombreuses pathologies rétiniennes dont les maladies vasculaires et tout particulièrement la rétinopathie diabétique. La possibilité d’accéder avec une facilité déconcertante à la rétine périphérique permet de mieux analyser les lésions avec un champ d’exploration de 200° soit une exploration de plus de 80 % de la rétine.
L’angiographie en fluorescence met en évidence l’étendue des territoires de non perfusion ou la présence de néovaisseaux prérétiniens non accessibles avec des appareils standards.
Le diagnostic de la rétinopathie diabétique est amélioré et de nombreuses publications viennent montrer l’intérêt de cette nouvelle technique d’imagerie qui pourrait à terme, modifier les classifications et optimiser la prise en charge des patients diabétiques.

Il y a quelques années l’arrivée des anti-VEGF nous a…
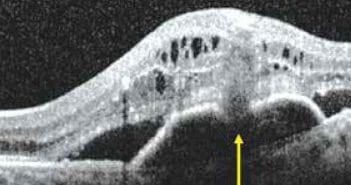
Les anastomoses choriorétiniennes (ACR) sont une des formes de néovascularisation compliquant la dégénérescence maculaire liée à l’âge. Elles représentent environ 15 % des néovaisseaux. Sur le plan clinique, elles sont souvent associées à des pseudodrusen réticulés, sont volontiers bilatérales et associées à un décollement de l’épithélium pigmentaire. Les formes évoluées peuvent ainsi se compliquer de déchirures de l’épithélium pigmentaire. La présence et l’extension de plages d’atrophie géographique sont également plus fréquentes dans les ACR. L’examen le plus performant pour les diagnostiquer est l’angiographie au vert d’indocyanine. L’examen en tomographie par cohérence optique (OCT) apporte néanmoins des informations utiles et permet souvent de visualiser les ACR et de les grader. L’OCT est également indispensable au suivi des ACR traitées. Le traitement de première intention des ACR repose sur les injections intravitréennes d’anti-VEGF.
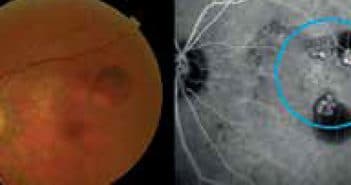
En rétine médicale, l’utilisation de la photothérapie dynamique (PDT) a révolutionné la prise en charge des patients atteints de néovaisseaux choroïdiens rétrofovéolaires exsudatifs : grâce à son effet photochimique sélectif sur les membranes néovasculaires sans destruction de la rétine sensorielle avoisinante, le prognostic fonctionnel visuel de ces patients pouvait être préservé.
Depuis l’avènement des anti-VEGF, même si elle bénéficie toujours d’une autorisation de mise sur le marché (AMM) dans la DMLA exsudative et le traitement des néovaisseaux du myope fort, la PDT a été reléguée au deuxième plan dans l’arsenal thérapeutique de ces affections. Elle garde pour
autant une place très pertinente dans certaines indications qui sont hors AMM, telle la choriorétinite séreuse centrale.
La PDT peut être utilisée seule ou combinée avec les anti-VEGF, par exemple dans la vasculopathie polypoïdale. De nombreux travaux ont montré une meilleure tolérance d’une réalisation de la PDT en demi-fluence ou demi-dose sans perte d’efficacité, en particulier dans ces indications.
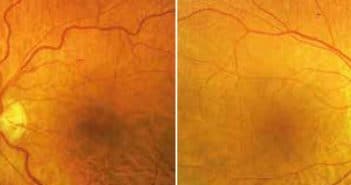
Les œdèmes papillaires (OP) et les occlusions veineuses rétiniennes (OVR) sont deux entités cliniques différentes, mais qui peuvent dans certains cas être associées. La turgescence des axones du nerf optique au sein d’un canal scléral rigide entraîne des modifications vasculaires, notamment un ralentissement de la circulation veineuse rétinienne.
Dans les occlusions de la veine centrale de la rétine (OVCR), la stase veineuse engendre une hypoxie et une rupture de la barrière hématorétinienne à l’origine parfois d’un OP. Nous nous intéresserons d’une part aux signes cliniques orientant vers une occlusion veineuse rétinienne face à un OP, d’autre part aux modifications veineuses résultant d’un OP.
